입력 : 2024-01-11 18:52:54
연세대학교(총장 서승환)는 본교 공과대학 신소재공학과 임용범 교수와 생명시스템대학 생명공학과 권호정 교수 연구팀이 가톨릭대 의과대학 구희범 교수 연구팀과 공동 연구를 통해 낮은 약물동태학 특성을 보이는 기존 펩타이드 약물의 단점을 보완할 수 있는 나노바이오 소재를 개발했다고 11일 밝혔다.
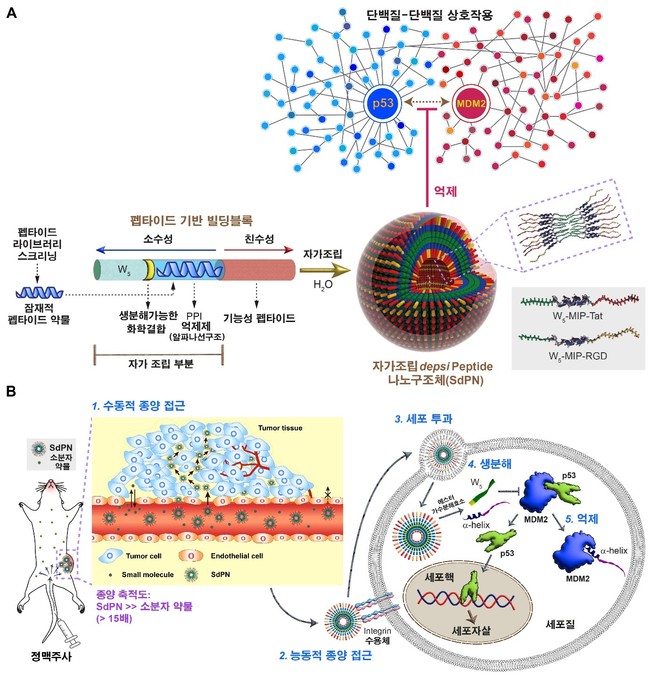
연구팀에 따르면 이번에 개발한 자가조립 뎁시펩타이드 나노구조체(Self-assembling Depsipeptide Nanostructure, SdPN)는 높은 생체 안정성과 암 조직 타겟팅 능력을 가지며, 세포 안에 도달하면 주위의 환경을 인식한 후 자동으로 생분해돼 ‘단백질-단백질 상호 작용(Protein-protein Interaction, PPI)’을 저해하는 항암 펩타이드를 방출하는 스마트 약물 전달 시스템이다.
세포 내 신호 전달에 관여하는 PPI는 유망한 약물 타깃으로 알려져 있지만, 구조적 특성과 좋지 않은 약물동태학적 특성으로 인해 상용화가 쉽지 않았다.
이를 해결하기 위해, 연구팀은 PPI를 억제할 수 있는 알파 나선을 포함하는 SdPN을 개발했다. 이 구조체는 체내에서 자가조립을 유도하는 소수성 코어 부분과 에스테르 결합으로 연결돼 세포 내 전달 이후 생분해를 통해 방출될 수 있는 알파 나선 펩타이드 약물 부분 그리고 세포 투과 펩타이드 부분으로 이뤄졌다.
알파 나선 펩타이드 약물 부분은 핫스폿이 주로 소수성 잔기로 이뤄져 있다는 것에 착안해, 자가조립 과정에 참여하게 디자인했으며, 합성한 펩타이드를 물에 녹이면 자가조립을 통해 자동적으로 분자들이 모여 나노캡슐 모양의 구조를 만드는 것을 검증했다.
해당 구조체의 알파 나선 펩타이드 약물 부분은 암세포의 세포 자살에 관련된 p53과 MDM2 간 상호 작용을 억제하는 MIP(MDM2 Inhibitory Peptide)로 구성했으며, 동물 실험 결과, 기존의 소분자 약물 대비 고효율로 종양에 전달돼 강한 항암 효과를 보이는 것을 연구팀은 확인했다.
연세대 임용범 교수는 “그간 많은 의구심 있었던 나노 약물에 대한 가능성이, 코로나 mRNA 나노 백신의 성공으로 명확히 입증됐다.”라며, “추가 연구개발을 통해 신개념 항암제 및 PPI 관련한 수많은 질병에 적용 가능한 나노 약물을 개발하고, 산업화도 추진할 계획이다.”라고 연구 의의를 밝혔다.
이번 논문은 연세대 최세환, 황현석, 가톨릭대 한성령 연구원이 공동 제1저자로, 연세대 엄호현, 최준식, 한상헌, 이수연, 가톨릭대 이동현 연구원이 공동저자로, 연세대 임용범 교수, 권호정 교수, 가톨릭대 의과대학 구희범 교수가 교신저자로 참여했으며, 한국연구재단, 연세대 ICONS 사업, 가톨릭교육재단의 연구비 지원으로 진행됐다.
본 논문은 약물 전달 분야 학술지 ‘Journal of Controlled Release (IF=10.8, JCR 상위 3.9%)’ 2024년 1월에 논문 제목 ‘Inhibition of protein-protein interactions using biodegradable depsipeptide nanoassemblies’으로 게재됐다.
베타뉴스 강규수 기자 ()
Copyrights ⓒ BetaNews.net
-
 목록
목록-
 위로
위로